活细胞和组织从周围环境中吸收各种化合物的能力很强。虽然细胞和组织对小分子的吸收相当简单,但吸收大分子就变得更加困难了。为了做到这一点,细胞必须使用特定的运输方式,其中之一就是内吞作用。
分子越大,就越难吸收,也就越难在细胞内运输。这使得大分子的输送,甚至是像药物这样具有生物重要性的大分子,成为一项研究挑战。除了发现新的有效方法将特定化合物送入细胞外,研究人员还寻找新的方法来量化这一过程,即提供进入细胞的分子数量及其进入时间等参数。最近,由Robert Ho?yst教授领导的波兰科学院物理化学研究所的研究人员展示了一种新的定量方法,以转铁蛋白摄取为例来描述内吞过程。让我们来仔细看看他们的发现。
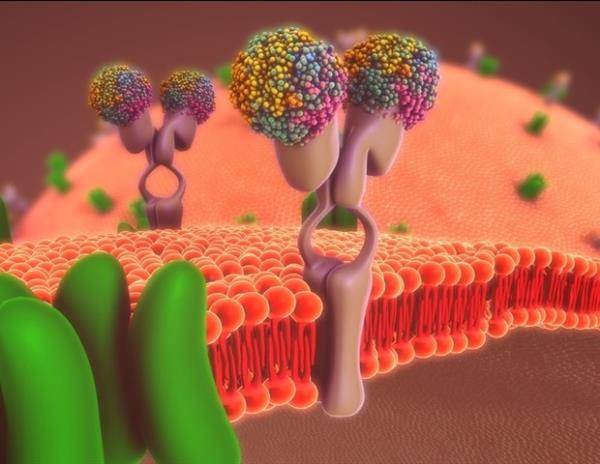
每个细胞都被一种叫做细胞膜的屏障与外界环境隔开,这种屏障保护细胞不受外界环境的影响。然而,这种屏障可以被某些维持细胞基本功能的化学物质所克服。物质穿过细胞膜进入或离开细胞的运动被称为细胞运输,虽然效率很高,但有时需要额外的因素,如蛋白质,它是一种特定化学物质的受体,作为进入细胞的“命名门票”。我们可以称之为内吞作用,这是细胞吸收分子或化合物的过程。换句话说,在这个过程中,大分子只有被捕获并包裹在膜结合载体内才能进入细胞。细胞使用许多不同的机制进行内吞作用。在网格蛋白介导的胞吞作用中,细胞表面受体选择性地结合集中在表面被涂坑中的大分子。接下来,它们相互挤压,形成包裹着网格蛋白的囊泡,这些囊泡将货物运送到细胞内部。这样,营养物质的吸收和细胞信号传递就会发生。它是如何工作的?
在人类细胞中,单个蛋白质可以在每个细胞中存在数个甚至数千万个拷贝。这使得观察这样一个复杂而具有挑战性的过程,为了观察涉及多种蛋白质的机制,人们需要足够灵敏的测量方法来检测单个分子。观察细胞内分子的标准方法是用荧光显微镜成像。这种方法被广泛使用,也非常有用,但它只允许像二元系统一样的观察——无论某物是否在细胞内,而且只有在超过一定的分子限制之后,才能确定这些物体有多少。
由Robert Ho?yst教授领导的波兰科学院物理化学研究所的研究人员开发的方法解决了这些限制。研究人员使用基于单光子计数的检测方法——光子是构成光的基本单位——我们可以看到单个粒子并对它们进行计数。科学家们校准了他们的设备,准备测量分子亮度,并消除背景中的光。通过这种测量,他们了解了一个分子发射出多少光子。
他们在研究中使用了转铁蛋白。为什么要在研究中使用这种特殊的分子?转铁蛋白是一种可逆结合铁的糖蛋白,负责铁在人体内的运输。对于在铁运输中的这种货物作用,转铁蛋白已经通过不同的方法进行了广泛的研究,因此用所提出的方法获得的结果可以与现有的文献数据进行比较。内吞作用是一个多步骤的过程,数十种不同的蛋白质以高度协调的方式共同作用,驱动内吞囊泡的形成。考虑到这个过程的复杂性,它需要多长时间?需要几秒钟还是几分钟?另外,为什么计算时间很重要?内吞作用除了为细胞吸收营养物质提供一种机制外,还是许多药物的主要进入途径。因此,通过确定时间分辨率等方法来了解内吞作用有助于开发不同的治疗策略。
该研究的第一作者Marta Pilz博士说:“我们的研究表明,单分子灵敏度荧光图像的定量分析是一种简单有效的工具,非常适合研究荧光分子的内吞作用。因此,我们预计定量成像将在评估药物输送效率方面发挥重要作用。”
作为一种方法,研究人员准备了独特的软件来分析荧光图像,并可能对单个分子发出的光子进行计数。应用这个系统,我们来测量细胞内较低的转铁蛋白浓度。由于软件和检测系统的创新组合,可以测量比以前使用的方法低100倍的细胞外浓度。因此,他们可以很容易地说明转铁蛋白是如何在细胞内积累的,以及它是否取决于外部浓度。
转铁蛋白周期时间——从转铁蛋白进入细胞到离开细胞的时间——是通过测量细胞转铁蛋白浓度随时间的变化来确定的。研究人员还观察到,循环时间不依赖于细胞外转铁蛋白的浓度。然而,细胞内的转铁蛋白浓度依赖于培养基中的转铁蛋白浓度。一旦超过一定的外部浓度,内部的值就不会增加。这是因为转铁蛋白需要前面提到的“票”,这是一种独特的受体,用于输入,其数量在细胞表面是有限的。IPC PAS科学家的研究表明,转铁蛋白受体的数量可以很容易地确定。此外,从细胞内外转铁蛋白浓度的依赖性出发,研究人员开发了一个数学公式,可以求解胞吞过程中不同步骤的时间。研究表明,转铁蛋白在细胞外停留的时间是由游离受体在细胞表面的搜寻时间、内化时间加上外部转铁蛋白浓度决定的。在足够高的转铁蛋白浓度下,大多数表面受体被占用,因此转铁蛋白必须等待一个自由的受体在循环完成后返回细胞表面。
为什么ICP PAS研究人员提出的方法很重要?所开发的方法,以及它在转铁蛋白运输的具体例子上的演示,显示了它在其他生物学问题上的潜在应用的可能性,例如,研究具有治疗特性的分子的运输,包括药物。该方法开辟了定量评估任何荧光分子进入活细胞的效率的可能性。也就是说,我们不仅可以知道某些物质是否存在于细胞中,还可以知道它进入和离开细胞的速度和数量。
“这里提出的结果表明,解决摄取测量挑战的综合方法能够量化活细胞中的内吞作用。通过定量荧光成像和由此产生的光子数矩阵,可以确定任何ROI(感兴趣区域)的浓度。因此,该方法可以平行测量细胞内外的浓度,并跟踪它们随时间的变化,正如这里通过对转铁蛋白摄取动力学的研究来提取转铁蛋白周期时间所示。”Marta Pilz博士评论道。
与现有方法相比,该方法具有较低的检测下限。此外,该过程对细胞是安全的,可以实现背景消除,并且可以实时(在实验期间)进行测量。
本研究在波兰科学基金、波兰虚拟研究所框架下发表于《塔兰塔》;grant WIB-1/2020-O11 - WIB_HERO。
为您推荐:
- 最新教程“奈曼麻将怎么开挂”分享用挂教程 2025-04-30
- “相当疯狂”:目击者详细描述了首席执行官枪击嫌疑人被捕的细节 2025-04-30
- 新方法改进了活细胞内吞作用的定量 2025-04-30
- 分享干货“微信小程序麻将开挂免费软件”真实有挂 2025-04-30
- 菲律宾团体提出弹劾副总统杜特尔特 2025-04-30
- 教程指点“丽水都莱开挂视频(真的有挂)-知乎 2025-04-30

